Axetilen là một chất trong hóa học. Nhưng khi học về axetilen rất nhiều em bỏ lỡ và rồi gặp khó khăn trong khi giải bài tập. Đã có nhiều em gửi thư về cho Tin Gen Z để xin hỗ trợ giải bài tập về axetilen. Chính vì thế, bài viết hôm nay chúng tôi sẽ giới thiệu về axetilen là gì? Công thức cấu tạo của axetilen? Cho một số bài tập về axetilen có lời giải dễ hiểu. Mời bạn đọc cùng đón xem trong bài viết dưới đây nhé.
Xem thêm:
- Oleum có công thức tổng quát là gì? Bài tập về Oleum
- Isopren là gì? Công thức cấu tạo của Isopren? Bài tập về Isopren
- Các Công Thức Tính Thế Năng Đơn Giản Và Bài Tập Có Lời Giải
- Cách tính phần trăm phiếu bầu đơn giản và chính xác nhất
Tìm hiểu về axetilen
Axetilen còn được gọi với tên khác là acetylene là chất khí, không màu, không mùi, nhẹ hơn không khí và nó ít tan trong nước.
Nó chính là một chất được sử dụng khá rộng rãi để làm nhiên liệu, để tổng hợp những hợp chất khác. Bởi vậy mà axetilen không tồn tại ở dạng tinh khiết hoàn toàn mà chỉ được để ở trong một dung dịch.
Công thức cấu tạo và phân tử của Axetilen
Axetilen có công thức phân tử là C2H2
Công thức cấu tạo của axetilen là H – C ≡ C – H và được viết ngắn gọn là HC ≡ CH.
Phân tử khối của axetilen là 26.
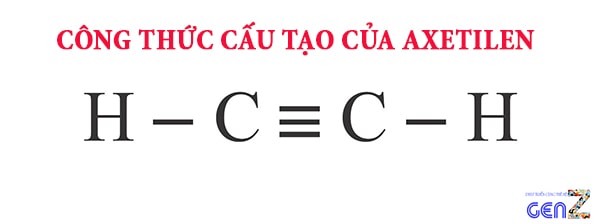
Đặc điểm cấu tạo của axetilen
- Trong công thức cấu tạo axetilen, giữa hai nguyên tử cacbon có 3 liên kết, nó được gọi là liên kết ba.
- Trong liên kết ba này lại có 2 liên kết kém bền, dễ bị đứt lần lượt trong những phản ứng hóa học hữu cơ. Bởi vậy, nó chính là yếu tố quyết định tính chất hóa học đặc trưng của axetilen.
Tính chất vật lý và tính chất hóa học của Axetilen
Tính chất vật lý
Axetilen là chất khí không có màu, không có mùi, nhẹ hơn không khí, dễ bắt cháy và ít được trong nước. Nó còn có tỉ trọng đối với không khí là D = 26/29. Nhưng trên thị trường hiện nay có rất nhiều loại có mùi lạ là bởi vì tạp chất gây ra.
Tính chất hóa học
- Tác dụng với oxi ta có:
2C2H2 + 5O2 + 4CO2 + 2H2O
- Phản ứng cộng với dd Brom ta có:
HC ≡ CH + Br2 → Br – CH = CH – Br (đibrometilen)
HC ≡ CH + 2Br2 → Br2CH – CHBr2 (tetrabrometan)
Bên cạnh đó, nếu trong điều kiện thích hợp thì axetilen còn có thể tham gia phản ứng cộng với rất nhiều loại chất khác như H2, Cl2…
Như vậy, có thể thấy axetilen rất tích cực trong hóa học. Bởi vậy mà lợi ích của nó đóng góp vào đời sống hàng ngày của con người rất nhiều.
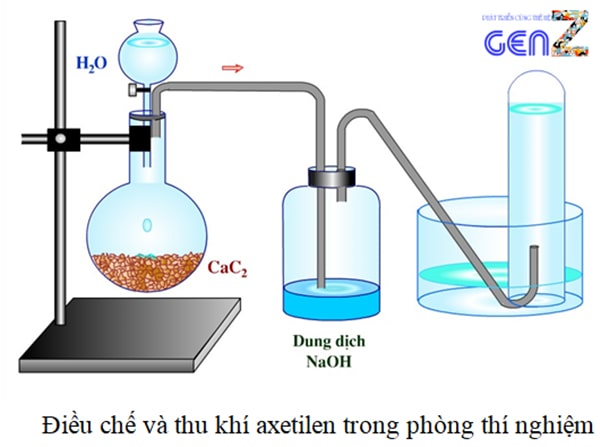
Cách điều chế Axetilen hiệu quả
- Trong phòng thí nghiệm và trong công nghiệp, cho canxi cacbua phản ứng với nước.
- Biện pháp hiện đại để có thể điều chế axetilen hiện đại là nhiệt phân metan ở nhiệt độ cao sau đó mới làm lạnh thật nhanh.
2CH4 → C2H2 + 3H2
1500oC
Một số ứng dụng của Axetilen
- Sử dụng axetilen trong đèn xì oxi – axetilen để hàn, cắt kim loại.
- Axetilen chính là nguyên liệu để sản xuất poli (vinyl clorua) dùng sản xuất nhựa PVC và nhiều loại hóa chất khác.
Những bài tập về Axetilen có lời giải dễ hiểu nhất
Bài tập 1: Cần bao nhiêu ml dung dịch Brom 0,1M để tác dụng vừa đủ với 0,334 lít axetilen ở điều kiện tiêu chuẩn?
Lời giải
nC2H2 = 0,334/22,4 = 0,01 mol
C2H2 + 2Br2 → C2H2Br4
1 mol 2 mol 1 mol
0,01 mol?
nBr2 = 2. nC2H2 = 0,02 (mol)
=> VBr2 = n/CM = 0,02/0,1 = 0,2 = 200 (ml)
Bài tập 2: Biết rằng 0,2 lít khí etilen (đktc) làm mất màu tối đa 60 ml dung dịch brom. Nếu dùng 0,2 khí axetilen (đktc) thì có thể làm mất màu tối đa bao nhiêu ml dung dịch brom trên?
Lời giải
Số mol của khí etilen nC2H4 = 0,2/22,4 = 0,009 (mol)
PTPU: CH2 = CH2 + Br2 → C2H4Br2 (1)
Theo PT ta có: 0,009 → 0,009 (mol)
HC ≡ CH + 2Br2 → Br2CH – CHBr2 (2)
0,009 → 20,1/22,4 (mol)
Từ (1) và (2) ta có số mol Br2 phản ứng với C2H2 gấp 2 lần số mol Br2 phản ứng với C2H4. Chính vì cùng một dung dịch Brom nên thể tích dung dịch brom cần là:
60 x 2 = 120 ml
Bài tập 3: Đốt cháy 29ml hỗn hợp khí metan và axetilen cần phải dùng 68,2 ml khí oxi. Tính phần trăm thể tích của mỗi khi có trong hỗn hợp?
Lời giải
Do những thể tích khí được đo ở cùng điều kiện nhiệt độ và áp suất nên tỉ lệ về thể tích cũng là tỉ lệ về số mol.
Gọi thể tích metan (CH4) là x, thể tích axetilen (C2H2) là y (ml)
Theo đề bài: Vhh khí = 29 ml
→ x + y = 29 ml (1)
PTPU: CH4 + 2O2 → CO2 + 2H2O
X → 2x → x (ml)
2C2H2 + 5O2 → 4CO2 + 2H2O
Y → 2,5y → 2y (ml)
Theo đề bài thì thể tích khí oxi là 68,2 ml
→ 2x + 2,5y = 68,2 ml (2)
Từ (1) và (2) giải HPT ta được:
X = 5,7 ml và y = 22,4 ml
Hy vọng bài viết trên của chúng tôi sẽ giúp bạn hiểu tổng quan toàn bộ kiến thức của axetilen. Nếu thấy hay thì hãy chia sẻ bài viết này đến bạn bè và người thân của bạn nhé, để các bạn học sinh cùng nhau học tập thật tốt nhé.
